Συγγραφέας:
Bobbie Johnson
Ημερομηνία Δημιουργίας:
10 Απρίλιος 2021
Ημερομηνία Ενημέρωσης:
1 Ιούλιος 2024

Περιεχόμενο
- Βήματα
- Μέρος 1 από 2: Προετοιμάστε τον εξοπλισμό
- Μέρος 2 από 2: Πραγματοποιήστε ένα πείραμα
- Συμβουλές
- Προειδοποιήσεις
- Τι χρειάζεσαι
Διαδικασία διάσπασης νερού (Η2Ο) στα συστατικά του (υδρογόνο και οξυγόνο) που χρησιμοποιούν ηλεκτρική ενέργεια ονομάζεται ηλεκτρόλυση. Τα αέρια που λαμβάνονται ως αποτέλεσμα της ηλεκτρόλυσης μπορούν να χρησιμοποιηθούν μόνα τους - για παράδειγμα, το υδρογόνο χρησιμεύει ως μία από τις πιο καθαρές πηγές ενέργειας. Ενώ το όνομα αυτής της διαδικασίας μπορεί να ακούγεται λίγο έξυπνο, είναι στην πραγματικότητα πιο εύκολο από ό, τι φαίνεται αν έχετε τον κατάλληλο εξοπλισμό, γνώσεις και λίγη εμπειρία.
Βήματα
Μέρος 1 από 2: Προετοιμάστε τον εξοπλισμό
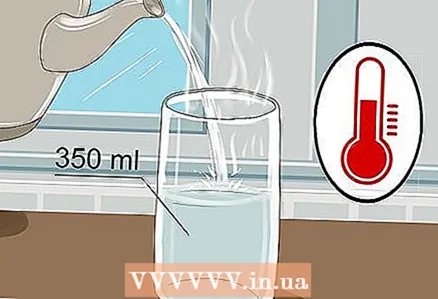 1 Πάρτε ένα ποτήρι 350 ml και ρίξτε χλιαρό νερό σε αυτό. Δεν χρειάζεται να γεμίσετε το ποτήρι μέχρι το χείλος, αρκεί λίγο νερό. Το κρύο νερό θα το κάνει, αν και το ζεστό νερό μεταφέρει καλύτερα τον ηλεκτρισμό.
1 Πάρτε ένα ποτήρι 350 ml και ρίξτε χλιαρό νερό σε αυτό. Δεν χρειάζεται να γεμίσετε το ποτήρι μέχρι το χείλος, αρκεί λίγο νερό. Το κρύο νερό θα το κάνει, αν και το ζεστό νερό μεταφέρει καλύτερα τον ηλεκτρισμό. - Και το νερό της βρύσης και το εμφιαλωμένο νερό θα κάνουν.
- Το ζεστό νερό έχει χαμηλότερο ιξώδες, γεγονός που διευκολύνει την κυκλοφορία των ιόντων.
 2 Διαλύστε 1 κουταλιά της σούπας (20 γραμμάρια) επιτραπέζιου αλατιού σε νερό. Ρίξτε αλάτι σε ένα ποτήρι και ανακατέψτε το νερό για να διαλυθεί. Αυτό θα δημιουργήσει αλατούχο διάλυμα.
2 Διαλύστε 1 κουταλιά της σούπας (20 γραμμάρια) επιτραπέζιου αλατιού σε νερό. Ρίξτε αλάτι σε ένα ποτήρι και ανακατέψτε το νερό για να διαλυθεί. Αυτό θα δημιουργήσει αλατούχο διάλυμα. - Το χλωριούχο νάτριο (δηλαδή το επιτραπέζιο άλας) είναι ένας ηλεκτρολύτης που αυξάνει την ηλεκτρική αγωγιμότητα του νερού. Από μόνο του, το νερό δεν μεταφέρει καλά την ηλεκτρική ενέργεια.
- Αφού αυξήσετε την ηλεκτρική αγωγιμότητα του νερού, το ρεύμα που δημιουργείται από την μπαταρία θα περάσει πιο εύκολα από το διάλυμα και θα διασπάσει αποτελεσματικότερα τα μόρια σε υδρογόνο και οξυγόνο.
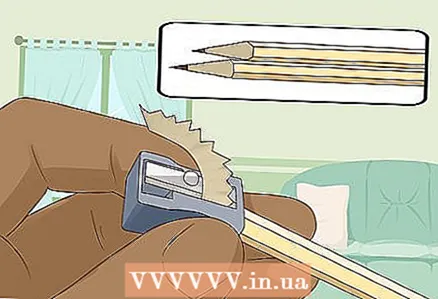 3 Ακονίστε δύο σκληρά μαλακά μολύβια και στα δύο άκρα για να εκθέσετε το μόλυβδο. Μην ξεχάσετε να αφαιρέσετε τη γόμα από τα μολύβια σας. Μια ράβδος γραφίτη πρέπει να προεξέχει και στα δύο άκρα.
3 Ακονίστε δύο σκληρά μαλακά μολύβια και στα δύο άκρα για να εκθέσετε το μόλυβδο. Μην ξεχάσετε να αφαιρέσετε τη γόμα από τα μολύβια σας. Μια ράβδος γραφίτη πρέπει να προεξέχει και στα δύο άκρα. - Οι ράβδοι γραφίτη θα χρησιμεύσουν ως μονωμένα ηλεκτρόδια στα οποία συνδέετε την μπαταρία.
- Ο γραφίτης είναι κατάλληλος για αυτό το πείραμα επειδή δεν διαλύεται ή διαβρώνεται στο νερό.
 4 Κόψτε ένα φύλλο χαρτονιού αρκετά μεγάλο για να τοποθετηθεί πάνω από το ποτήρι. Χρησιμοποιήστε ένα αρκετά παχύ κομμάτι χαρτόνι που δεν θα κρεμάσει αφού ανοίξετε δύο τρύπες σε αυτό. Κόψτε ένα τετράγωνο κομμάτι από ένα κουτί παπουτσιών ή κάτι παρόμοιο.
4 Κόψτε ένα φύλλο χαρτονιού αρκετά μεγάλο για να τοποθετηθεί πάνω από το ποτήρι. Χρησιμοποιήστε ένα αρκετά παχύ κομμάτι χαρτόνι που δεν θα κρεμάσει αφού ανοίξετε δύο τρύπες σε αυτό. Κόψτε ένα τετράγωνο κομμάτι από ένα κουτί παπουτσιών ή κάτι παρόμοιο. - Το χαρτόνι χρησιμοποιείται για να συγκρατεί τα μολύβια στο νερό, έτσι ώστε να μην αγγίζουν τις πλευρές και το κάτω μέρος του ποτηριού.
- Το χαρτόνι δεν είναι αγώγιμο, οπότε μπορείτε να το βάλετε με ασφάλεια σε ένα ποτήρι.
 5 Χρησιμοποιήστε μολύβια για να ανοίξετε δύο τρύπες στο χαρτόνι. Τρυπήστε το χαρτόνι με μολύβια - σε αυτή την περίπτωση, θα σφίξουν καλά και δεν θα γλιστρήσουν. Βεβαιωθείτε ότι ο γραφίτης δεν αγγίζει τις πλευρές ή το κάτω μέρος του γυαλιού, διαφορετικά θα παρεμβαίνει στο πείραμα.
5 Χρησιμοποιήστε μολύβια για να ανοίξετε δύο τρύπες στο χαρτόνι. Τρυπήστε το χαρτόνι με μολύβια - σε αυτή την περίπτωση, θα σφίξουν καλά και δεν θα γλιστρήσουν. Βεβαιωθείτε ότι ο γραφίτης δεν αγγίζει τις πλευρές ή το κάτω μέρος του γυαλιού, διαφορετικά θα παρεμβαίνει στο πείραμα.
Μέρος 2 από 2: Πραγματοποιήστε ένα πείραμα
 1 Συνδέστε ένα καλώδιο με συνδετήρες αλιγάτορα σε κάθε ακροδέκτη μπαταρίας. Η μπαταρία θα χρησιμεύσει ως πηγή ηλεκτρικού ρεύματος και μέσω των καλωδίων με σφιγκτήρες και ράβδους γραφίτη, το ρεύμα θα φτάσει στο νερό.Συνδέστε το ένα καλώδιο με έναν σφιγκτήρα στο θετικό και το άλλο στον αρνητικό ακροδέκτη της μπαταρίας.
1 Συνδέστε ένα καλώδιο με συνδετήρες αλιγάτορα σε κάθε ακροδέκτη μπαταρίας. Η μπαταρία θα χρησιμεύσει ως πηγή ηλεκτρικού ρεύματος και μέσω των καλωδίων με σφιγκτήρες και ράβδους γραφίτη, το ρεύμα θα φτάσει στο νερό.Συνδέστε το ένα καλώδιο με έναν σφιγκτήρα στο θετικό και το άλλο στον αρνητικό ακροδέκτη της μπαταρίας. - Χρησιμοποιήστε μπαταρία 6 volt. Εάν δεν έχετε, μπορείτε να χρησιμοποιήσετε μια μπαταρία 9 βολτ αντ 'αυτού.
- Μπορείτε να προμηθευτείτε μια κατάλληλη μπαταρία από ένα κατάστημα ηλεκτρικών ειδών ή ένα σούπερ μάρκετ.
 2 Συνδέστε τις άλλες άκρες των καλωδίων με τα μολύβια. Συνδέστε τους μεταλλικούς σφιγκτήρες σύρματος σταθερά στις ράβδους γραφίτη. Σως χρειαστεί να αφαιρέσετε λίγο ξύλο από τα μολύβια για να μην γλιστρήσουν τα κλιπ από τις ράβδους γραφίτη.
2 Συνδέστε τις άλλες άκρες των καλωδίων με τα μολύβια. Συνδέστε τους μεταλλικούς σφιγκτήρες σύρματος σταθερά στις ράβδους γραφίτη. Σως χρειαστεί να αφαιρέσετε λίγο ξύλο από τα μολύβια για να μην γλιστρήσουν τα κλιπ από τις ράβδους γραφίτη. - Έτσι, θα κλείσετε το κύκλωμα και το ρεύμα από την μπαταρία θα ρέει μέσα στο νερό.
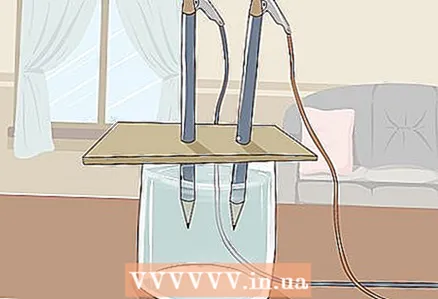 3 Τοποθετήστε το χαρτόνι στο ποτήρι έτσι ώστε τα ελεύθερα άκρα των μολυβιών να βυθιστούν στο νερό. Το φύλλο από χαρτόνι πρέπει να είναι αρκετά μεγάλο για να ακουμπάει στο γυαλί. Προσέξτε να μην διαταράξετε τη σωστή τοποθέτηση των μολυβιών.
3 Τοποθετήστε το χαρτόνι στο ποτήρι έτσι ώστε τα ελεύθερα άκρα των μολυβιών να βυθιστούν στο νερό. Το φύλλο από χαρτόνι πρέπει να είναι αρκετά μεγάλο για να ακουμπάει στο γυαλί. Προσέξτε να μην διαταράξετε τη σωστή τοποθέτηση των μολυβιών. - Για να είναι επιτυχές το πείραμα, ο γραφίτης δεν πρέπει να αγγίζει τους τοίχους και το κάτω μέρος του γυαλιού. Ελέγξτε ξανά αυτό και ρυθμίστε τα μολύβια εάν είναι απαραίτητο.
 4 Παρακολουθήστε το νερό να χωρίζεται σε υδρογόνο και οξυγόνο. Οι φυσαλίδες αερίου θα αρχίσουν να ανεβαίνουν από τις ράβδους γραφίτη βυθισμένες στο νερό. Αυτά είναι υδρογόνο και οξυγόνο. Το υδρογόνο θα απελευθερωθεί στον αρνητικό πόλο και το οξυγόνο στο θετικό πόλο.
4 Παρακολουθήστε το νερό να χωρίζεται σε υδρογόνο και οξυγόνο. Οι φυσαλίδες αερίου θα αρχίσουν να ανεβαίνουν από τις ράβδους γραφίτη βυθισμένες στο νερό. Αυτά είναι υδρογόνο και οξυγόνο. Το υδρογόνο θα απελευθερωθεί στον αρνητικό πόλο και το οξυγόνο στο θετικό πόλο. - Μόλις συνδέσετε τα καλώδια με την μπαταρία και τις ράβδους γραφίτη, ένα ηλεκτρικό ρεύμα θα ρέει μέσα στο νερό.
- Περισσότερες φυσαλίδες αερίου θα σχηματιστούν στο μολύβι που συνδέεται με τον αρνητικό πόλο, αφού κάθε μόριο νερού αποτελείται από δύο άτομα υδρογόνου και ένα άτομο οξυγόνου.
Συμβουλές
- Εάν δεν έχετε μολύβια με άξονες γραφίτη, μπορείτε να χρησιμοποιήσετε δύο μικρά καλώδια. Απλώς τυλίξτε το ένα άκρο κάθε σύρματος γύρω από τον αντίστοιχο πόλο μπαταρίας και βυθίστε το άλλο στο νερό. Το αποτέλεσμα θα είναι το ίδιο με τα μολύβια.
- Δοκιμάστε να χρησιμοποιήσετε διαφορετική μπαταρία. Η ποσότητα του ρεύματος που ρέει εξαρτάται από την τάση της μπαταρίας, η οποία, με τη σειρά της, επηρεάζει το ρυθμό διάσπασης των μορίων νερού.
Προειδοποιήσεις
- Εάν προσθέσετε έναν ηλεκτρολύτη, όπως το αλάτι, στο νερό, λάβετε υπόψη ότι το πείραμα θα δημιουργήσει μια μικρή ποσότητα ενός υποπροϊόντος όπως το χλώριο. Είναι ασφαλές σε τόσο μικρές ποσότητες, αλλά μπορείτε να μυρίσετε μια μικρή μυρωδιά χλωρίου.
- Πραγματοποιήστε αυτό το πείραμα υπό την επίβλεψη ενηλίκων. Συνδέεται με τον ηλεκτρισμό και τα αέρια και ως εκ τούτου μπορεί να είναι επικίνδυνο, αν και απίθανο.
Τι χρειάζεσαι
- Δύο σκληρά μαλακά μολύβια
- Μία μπαταρία 6 ή 9 βολτ
- Γυαλί με όγκο 350 χιλιοστόλιτρα
- 2 σύρματα με κλιπ κροκόδειλου
- Ακονιστής για μολύβι
- Αλας