Συγγραφέας:
John Pratt
Ημερομηνία Δημιουργίας:
17 Φεβρουάριος 2021
Ημερομηνία Ενημέρωσης:
26 Ιούνιος 2024

Περιεχόμενο
- Για να πας
- Μέθοδος 1 από 2: Υπολογισμός της μοριακής μάζας ενός στοιχείου
- Μέθοδος 2 από 2: Υπολογισμός της μοριακής μάζας μιας σύνθετης ουσίας
- Συμβουλές
- Προειδοποιήσεις
- Απαιτήσεις
Τα άτομα είναι πολύ μικρά για σημαντικές μετρήσεις χημικών. Για να μπορέσουμε να εργαστούμε με πολύ μικρές ποσότητες μιας συγκεκριμένης ουσίας, αυτές ταξινομούνται από τους επιστήμονες σε μονάδες mol. Το mole ορίζεται ως μια ορισμένη ποσότητα ουσίας με τόσα σωματίδια όπως ο αριθμός των ατόμων άνθρακα σε 12 γραμμάρια του ισοτόπου C-12, που ισοδυναμεί με περίπου 6.022 14 × 10. Αυτό ονομάζεται αριθμός Avogadro ή σταθερά. Χρησιμοποιείται για να δείξει τον αριθμό ατόμων, μορίων, ιόντων ή υποατομικών σωματιδίων σε οποιαδήποτε ουσία και η μάζα 1 mole είναι η μοριακή μάζα αυτής της ουσίας. Εδώ μπορείτε να διαβάσετε πώς να υπολογίσετε τη μοριακή μάζα στοιχείων και ουσιών.
Για να πας
Μέθοδος 1 από 2: Υπολογισμός της μοριακής μάζας ενός στοιχείου
 Βρείτε τη σχετική ατομική μάζα του στοιχείου. Η σχετική ατομική μάζα ενός στοιχείου είναι ο σταθμισμένος μέσος όρος, εκφρασμένος σε μονάδες ατομικής μάζας (u), των ατομικών μαζών όλων των φυσικών ισοτόπων. Αυτές οι πληροφορίες βρίσκονται στον περιοδικό πίνακα. Για παράδειγμα, το υδρογόνο έχει σχετική ατομική μάζα 1,008. άνθρακας 12.0107; οξυγόνο 15.9994; και χλώριο 35,453.
Βρείτε τη σχετική ατομική μάζα του στοιχείου. Η σχετική ατομική μάζα ενός στοιχείου είναι ο σταθμισμένος μέσος όρος, εκφρασμένος σε μονάδες ατομικής μάζας (u), των ατομικών μαζών όλων των φυσικών ισοτόπων. Αυτές οι πληροφορίες βρίσκονται στον περιοδικό πίνακα. Για παράδειγμα, το υδρογόνο έχει σχετική ατομική μάζα 1,008. άνθρακας 12.0107; οξυγόνο 15.9994; και χλώριο 35,453. 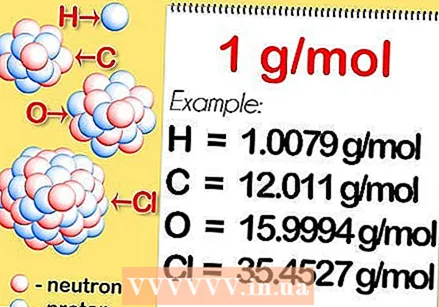 Πολλαπλασιάστε με τη μοριακή μάζα. Αυτό ορίζεται ως 1 γραμμάριο ανά γραμμομόριο. Αυτό μετατρέπει τη μονάδα ατομικής μάζας σε γραμμάρια ανά γραμμομόριο, καθιστώντας τη γραμμομοριακή μάζα υδρογόνου ίση με 1,008 γραμμάρια ανά γραμμομόριο, άνθρακα 12,0107 γραμμάρια ανά γραμμομόριο, οξυγόνο 15,9994 γραμμάρια ανά γραμμομόριο και χλώριο 35,453 γραμμάρια ανά γραμμομόριο.
Πολλαπλασιάστε με τη μοριακή μάζα. Αυτό ορίζεται ως 1 γραμμάριο ανά γραμμομόριο. Αυτό μετατρέπει τη μονάδα ατομικής μάζας σε γραμμάρια ανά γραμμομόριο, καθιστώντας τη γραμμομοριακή μάζα υδρογόνου ίση με 1,008 γραμμάρια ανά γραμμομόριο, άνθρακα 12,0107 γραμμάρια ανά γραμμομόριο, οξυγόνο 15,9994 γραμμάρια ανά γραμμομόριο και χλώριο 35,453 γραμμάρια ανά γραμμομόριο. - Βρείτε τη μοριακή μάζα ενός δισθενούς μορίου. Ορισμένα στοιχεία μπορούν να βρεθούν μόνο σε μόρια των 2 ή περισσότερων. Αυτό σημαίνει ότι εάν θέλετε να υπολογίσετε τη μοριακή μάζα ενός στοιχείου που, για παράδειγμα, αποτελείται από 2 άτομα, όπως υδρογόνο, οξυγόνο και χλώριο, προσδιορίστε τη σχετική ατομική μάζα και πολλαπλασιάστε την με τη μοριακή μάζα και πολλαπλασιάστε την αποτέλεσμα από 2.
- Η μοριακή μάζα ενός στοιχείου είναι τότε ίση με τη μοριακή μάζα ενός ατόμου επί τον αριθμό των ατόμων σε κάθε μόριο: στην περίπτωση του υδρογόνου, 1,008 φορές 2, ή 2,016 γραμμάρια ανά γραμμομόριο. οξυγόνο, 15,9994 φορές 2 ή 31,9988 γραμμάρια ανά γραμμομόριο. και με χλώριο, 35,453 φορές 2, ή 70,096 γραμμάρια ανά γραμμομόριο.
Μέθοδος 2 από 2: Υπολογισμός της μοριακής μάζας μιας σύνθετης ουσίας
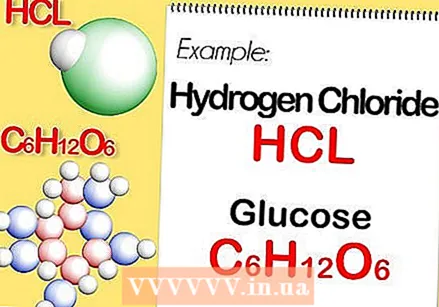 Προσδιορίστε τον χημικό τύπο της ένωσης. Αυτός είναι ο αριθμός των ατόμων σε κάθε στοιχείο της ένωσης. (Θα βρείτε πληροφορίες σχετικά με αυτό, για παράδειγμα, στο Binas) Για παράδειγμα: ο τύπος για το υδροχλώριο (υδροχλωρικό οξύ) είναι HCl. για γλυκόζη C6Η.12Ο6. Ο τελευταίος τύπος σημαίνει ότι η γλυκόζη περιέχει 6 άτομα άνθρακα, 12 άτομα υδρογόνου και 6 άτομα οξυγόνου.
Προσδιορίστε τον χημικό τύπο της ένωσης. Αυτός είναι ο αριθμός των ατόμων σε κάθε στοιχείο της ένωσης. (Θα βρείτε πληροφορίες σχετικά με αυτό, για παράδειγμα, στο Binas) Για παράδειγμα: ο τύπος για το υδροχλώριο (υδροχλωρικό οξύ) είναι HCl. για γλυκόζη C6Η.12Ο6. Ο τελευταίος τύπος σημαίνει ότι η γλυκόζη περιέχει 6 άτομα άνθρακα, 12 άτομα υδρογόνου και 6 άτομα οξυγόνου. 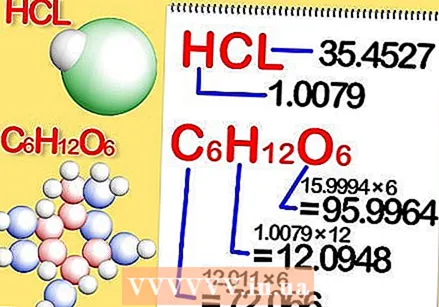 Προσδιορίστε τη μοριακή μάζα κάθε στοιχείου στην ένωση. Πολλαπλασιάστε την ατομική μάζα του στοιχείου με τη μοριακή μάζα και τον αριθμό των ατόμων του στοιχείου στην ένωση. Δείτε πώς λειτουργεί:
Προσδιορίστε τη μοριακή μάζα κάθε στοιχείου στην ένωση. Πολλαπλασιάστε την ατομική μάζα του στοιχείου με τη μοριακή μάζα και τον αριθμό των ατόμων του στοιχείου στην ένωση. Δείτε πώς λειτουργεί: - Η γραμμομοριακή μάζα κάθε στοιχείου υδροχλωρίου, HCl, είναι 1,008 γραμμάρια ανά γραμμομόριο υδρογόνου και 35,453 γραμμάρια ανά γραμμομόριο χλωρίου.
- Η μοριακή μάζα κάθε στοιχείου γλυκόζης, C.6Η.12Ο6, είναι 12.0107 φορές 6, ή 72.0642 γραμμάρια ανά γραμμομόριο άνθρακα. 1,008 φορές 12 ή 12,096 γραμμάρια ανά γραμμομόριο υδρογόνου. και 15,994 φορές 6, ή 95,9964 γραμμάρια ανά γραμμομόριο οξυγόνου.
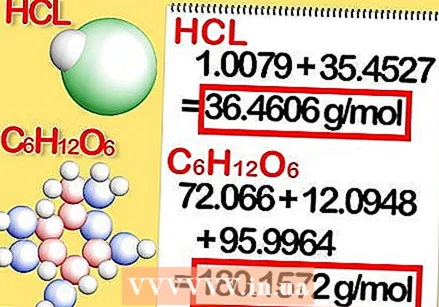 Προσθέστε τις μοριακές μάζες κάθε στοιχείου στην ένωση. Αυτό δίνει τη μοριακή μάζα της ένωσης. Δείτε πώς:
Προσθέστε τις μοριακές μάζες κάθε στοιχείου στην ένωση. Αυτό δίνει τη μοριακή μάζα της ένωσης. Δείτε πώς: - Η γραμμομοριακή μάζα του υδροχλωρίου είναι 1,008 + 35,453 ή 36,461 γραμμάρια ανά γραμμομόριο.
- Η γραμμομοριακή μάζα της γλυκόζης είναι 72,0642 + 12,096 + 95,9964 ή 180,1566 γραμμάρια ανά γραμμομόριο.
Συμβουλές
- Ενώ στις περισσότερες περιπτώσεις οι σχετικές ατομικές μάζες έχουν ακρίβεια 4 δεκαδικών ψηφίων, στο εργαστήριο μια ακρίβεια 2 δεκαδικών ψηφίων ή λιγότερο ισχύει για εξαιρετικά μεγάλες μάζες. Έτσι, στο εργαστήριο, η γραμμομοριακή μάζα του υδροχλωρίου είναι 36,46 γραμμάρια ανά γραμμομόριο και αυτή της γλυκόζης είναι 180,16 γραμμάρια ανά γραμμομόριο.
Προειδοποιήσεις
- Μην συγχέετε τη μοριακή μάζα και τη μοριακή μάζα. Το τελευταίο είναι η μάζα ενός μεμονωμένου μορίου ενός στοιχείου ή μιας ένωσης. Η μοριακή μάζα μπορεί να γίνει κατανοητή ως η μέση μάζα όλων των μορίων σε ένα δείγμα μιας συγκεκριμένης ουσίας, όπως και η σχετική ατομική μάζα είναι ο μέσος όρος των ατομικών μαζών όλων των ισοτόπων.
Απαιτήσεις
- Κάδοι και περιοδικός πίνακας των στοιχείων
- Αριθμομηχανή